| 临床级VIRUS-Free™技术:
致敬伟大的芭芭拉·麦克林托克,她发现的转座子机制在我们这个时代,依然是一个非常出色的基因研究工具!芭芭拉·麦克林托克(英语:Barbara McClintock)1983年获得诺贝尔生理学或医学奖,是首位没有共同得奖者的女科学家。
——VIRUS-Free™ 技术研究团队
在过表达稳定细胞株构建技术基本被病毒法垄断的时候,其实还有一个很重要的技术在不断的进化中!如今该技术又再一次走人了人们的视野:VIRUS-Free™基于转座子系统的稳转细胞系构建技术,该技术目前已经有多个临床项目在进行中,包括了CAR-T细胞和很多细胞基因编辑临床项目。
而回望这个技术的研发之路确实不平坦,就如这个技术的出生一样,芭芭拉不知道受到了多少的白眼和非议,但是迟来的诺奖却给予了她肯定。
| 由于我们研发的定位要素包括:
1. 低成本(目前CAR-T的问题就是价格高)
2. 表达稳定可控(临床应用肯定要在体内多次分裂不丢失)
3. 序列完整,没有其他蛋白结构产生;
4. 可移除(稳转之后可以移除)
| 而这个目标基本是病毒法无法达到的:
1. 病毒很容易受到免疫抑制或者其启动子受到影响,在多代之后沉默不表达;
2. 病毒表达蛋白的完整性受到病毒包装过程的载体质量的影响;
3. 不可能移除;
4. 插入拷贝数不确定,表达克隆差异很大;
5. 片段大小非常有限;
所以我们聚焦到了:转座子系统,而其中的困难就是对转座子载体的研发上。具体过程涉及多项研发的核心内容,就不过多透露。
经过两年的开发:我们推出了VIRUS-Free™ 技术,正好可以完美的满足我们的需求,下面是关于技术的介绍材料:
| 技术优势:
1.序列完整性好,如果小环的结构被破坏则无法实现基因组插入;
2.可插入大片段,可以实现上百Kb的BAC片段的插入,而且能够保证其序列完整性,可以进行复杂的基因功能研究;
3.目的插入效率高,由于通过酶促反应,所以整个反应的过程效率远远高于DNA随机插入效率;
4.目的基因表达稳定,由于细胞插入的拷贝数相对于病毒来说比较稳定,在稳转株的构建过程中,细胞的表达更加稳定;
5.实验时间只需要慢病毒系统时间一半,实验更加安全;
6.可以实现:稳转之后对目的克隆进行检测后可以再将目的基因在原克隆移除,轻松实现加减法的对照。
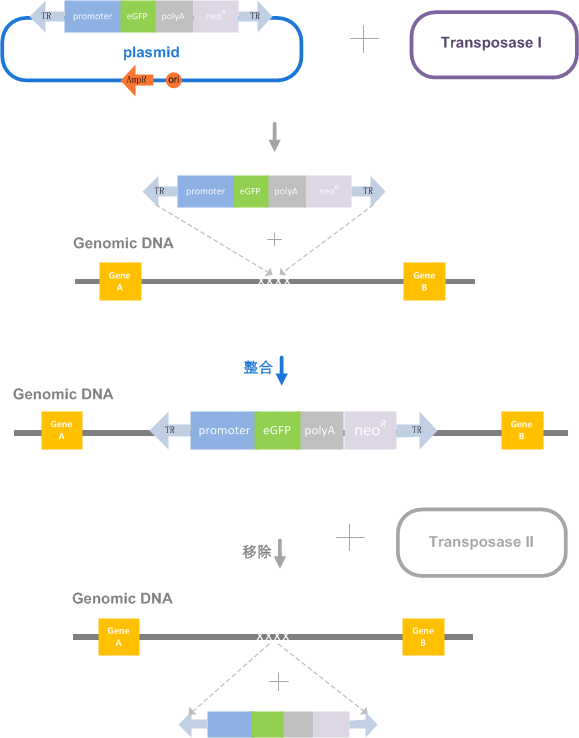
| 技术流程图:

| VIRUS-Free™ 细胞基因稳转技术
2Kb以内基因插入(合成法)
插入片段小于2Kb的项目,我们将通过化学合成的办法获得质粒,并进行细胞转导,通过抗药性的筛选获得稳转克隆。
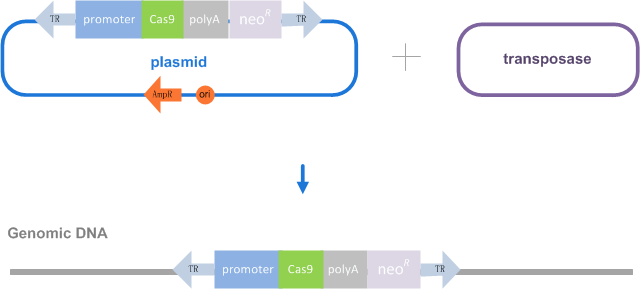
2-20Kb的基因插入(载体法)
插入片段2-8Kb的项目,我们将通过载体构建的办法来获得质粒,并进行细胞转导,通过抗药性的筛选获得稳转克隆。
Step1. 目的序列PCR扩增
Step2. 目的载体的构建获得表达载体
Step3. 目的细胞的转导和抗性药物筛选获得目的克隆
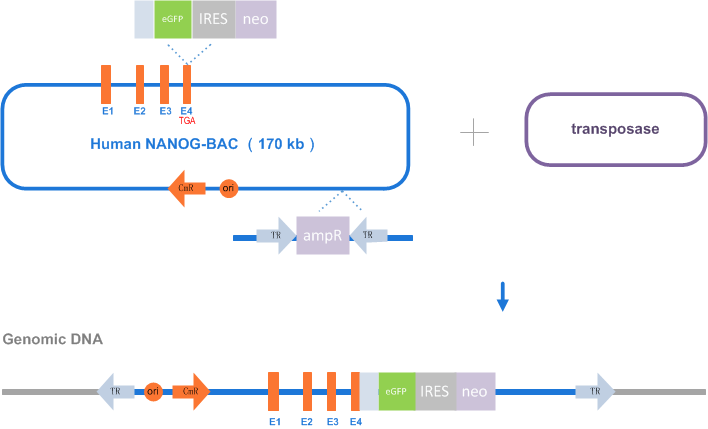
BAC片段细胞系稳转(BAC修饰):通过Red重组系统对BAC进行遗传修饰获得重组BAC,并进行细胞转导,通过抗药性的筛选获得稳转克隆。
Step1. 目的序列PCR扩增
Step2. 通过Red重组获得经过遗传修饰的BAC
Step3. 目的细胞的转导和抗性药物筛选获得目的克隆