

今天我们要讲的是生命科学发展的能工巧匠—基因编辑技术,该技术通过人为的对目的基因进行修饰,实现其编辑功能,从而达到改变目的细胞基因型的目的。
2020年的诺贝尔化学奖授予了詹妮弗·杜德纳(Jennifer Doudna)和艾曼纽·卡彭蒂耶(Emmanuelle Charpentier),以表彰他们对基因编辑技术CRISPR的研究成果。在CRISPER-Cas9技术开发之前,第一代锌指核酸酶(ZFNs)技术以及第二代转录激活因子效应物核酸酶(TALENs)已被广泛应用。三者的原理都是通过在基因组序列上诱导双链断裂(DSB),并随后通过内源性修复机制进行纠正,达到基因片段缺失、插入、突变等基因编辑的目的。
通过同源重组(HR)将内源性基因组序列与外源供体DNA分子进行交换是一个几十年前就已为人所知的过程。已故的奥利弗·史密斯(Oliver Smithies)首次阐明了同源DNA分子如何重组并正确插入哺乳动物染色体的特定位置。为此,史密斯与马里奥·卡佩基(Mario Capecchi)以及马丁·埃文斯(Martin Evans)共同获得了2007年的诺贝尔生理学或医学奖。

2009科学家首次使用ZFNs技术制造了世界上第一个基因敲除大鼠,1996年ZFNs技术被大力发展,该技术通过改造ZFN的结构域,可以人为设计识别特定DNA的ZFN并促使其与目的DNA序列进行结合,随后,核酸内切酶FOKI可对DNA双链进行切割形成DSB,最后完成DNA的自我修复。该技术在发展过程中有设计简单,效率较高的特点,但是随着科学的发展,人们发现其具有周期长、易脱靶 、细胞毒性大的缺点。
第二代基因编辑技术TALEN作为ZFNs的替代产品,在2021年进入快速开发期,2012年,科学杂志将TALEN技术列入了年度十大科学突破列表,TALE的全称是Transcription Activator-Like Effector,即转录激活因子样效应蛋白,来源于植物病原菌, TALEN技术的主要原理是通过两个TALE靶向识别靶点两侧的序列;每个TALE融合一个FokI内切酶结构域;FokI通过TALE靶向形成二聚体切割靶点,诱导双链断裂,促使DNA进行自我修复过程并最终达到基因编辑的目的,TALEN具有技术设计灵活识别特异性强的优点。
ZFNs用30个氨基酸组成一个对应三碱基的DNA识别结构域,而TALE蛋白用34个氨基酸组成一个仅精准对应一个碱基的DNA识别结构域。此外,相比于ZFNs技术,TALE有一个决定性的优点,就是可模块化,通过删减、添加、自由组合不同的TALE蛋白,就可以轻易地定位DNA片段,将基因编辑周期缩短。但是,用脂质体转染法还是电穿孔法转染细胞构建细胞系,病毒所能运送的DNA序列也是有限的,而使用病毒侵染法递送外援DNA进行基因治疗,转染效率也不可避免地与蛋白质大小成反比,所以太大的TALE无疑会导致DNA的切割效率降低。此外,该项技术也存在与ZFNs一样的脱靶率高,细胞毒性大的缺点。
不过,科学家们很快开发出了新一代基因编辑技术,相比于前两代技术更为高校、快捷。准确且价位低,那就是我们熟知的CRISPR/Cas9技术,主要组成部分是成簇的规律性间隔的短回文重复序列CRISPR以及核算内切酶Cas9组成, 2011年,CRISPR/Cas9系统的分子机制被揭示, 2014年,一位美国的生物化学家Jennifer首先阐明了CRISPR/Cas9系统的工作原理,证明它可以根据一段向导RNA(gRNA)的指引,找到对应的DNA序列,并将其切开。CRISPR/Cas9系统的工作原理是 crRNA通过碱基配对与 tracrRNA结合形成 tracrRNA/crRNA 复合物,此复合物引导核酸酶 Cas9 蛋白在与 crRNA 配对的序列靶位点剪切双链 DNA。而通过人工设计 crRNA 和 tracrRNA 这两种 RNA,改造成具有引导作用的sgRNA ,从而引导 Cas9 对 DNA 的定点切割。随后不久,MIT的华人生物学家张锋证明了这一系统同样可以在哺乳动物细胞中使用。CRISPR/Cas9系统是细菌和古菌特有的一种天然防御系统,用于抵抗病毒或外源性质粒的侵害。当外源基因入侵时,该防御系统的 CRISPR 序列会表达与入侵基因组序列相识别的 RNA,然后 CRISPR 相关酶在序列识别处切割外源基因组DNA,从而达到防御目的。
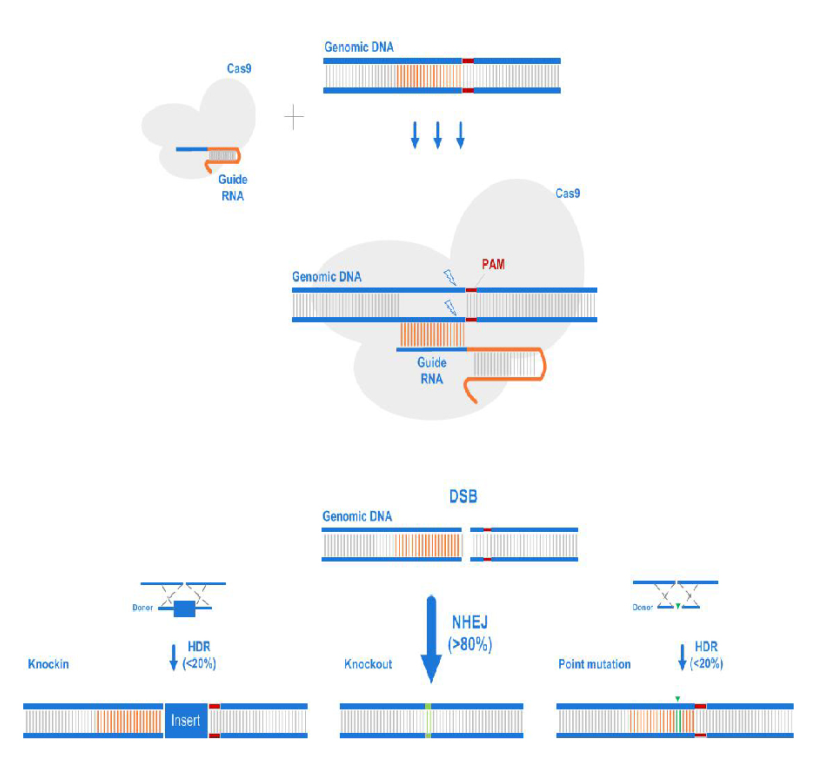
CRISPR/Cas9技术原理
1.sgRNA与Cas9蛋白结合,形成RNP复合物
2.RNP复合物在sgRNA的引导下,定位到基因组上的靶位点
3.Cas9蛋白对靶位点的DNA双链进行切割,产生双链断裂(DSB)
4.DSB引起细胞的紧急修复机制:非同源末端连接(NHEJ)修复或者同源重组修复(HDR)
5.绝大多数情况下(>80%),细胞采用NHEJ修复路径,使得靶位点位置随机产生个别碱基的删除或插入(Indel),得到基因敲除模型
6.极少数情况下(<20%),且细胞内存在同源片段时,细胞采用HDR修复路径,使得靶位点产生精确修复
7.在同源片段中引入外源基因片段或者突变碱基,可得到基因定点插入模型或者基因定点突变模型
近几年,CRISPR/Cas基因编辑技术飞速发展,涉及在生物、医学、农业以及环境等多个领域的应用, 2017年CRISPR/Cas9基因编辑技术应用于CAR-T疗法;杨璐菡等在Science发表文章,通过CRISPR/Cas9技术完成了对猪基因组中的内源逆转录病毒(PERV)序列的敲除。同年,杂交水稻之父”袁隆平院士宣布使用CRISPR/Cas9技术完成了对水稻中与镉吸收和积累相关的基因的敲除。
目前为止,关于CRISPR/Cas9技术的新突破不断涌现,相比于前两代基因编辑技术,CRISPR/Cas9技术切割效率极高,便利性强,ZFNs与TALENs需要用成百上千个碱基的长度来完成定位系统的组装,而CRISPR则只需要与目的基因一一对应的一段gRNA即可完成这个任务,且Cas9蛋白自己本身就具有核酸内切酶的活性,不需额外的核酸内切酶。为今后大范围治疗点突变遗传疾病提供了极大的便利。此外,该技术还有设计简单,能靶向几乎任意细胞任意序列的优点。
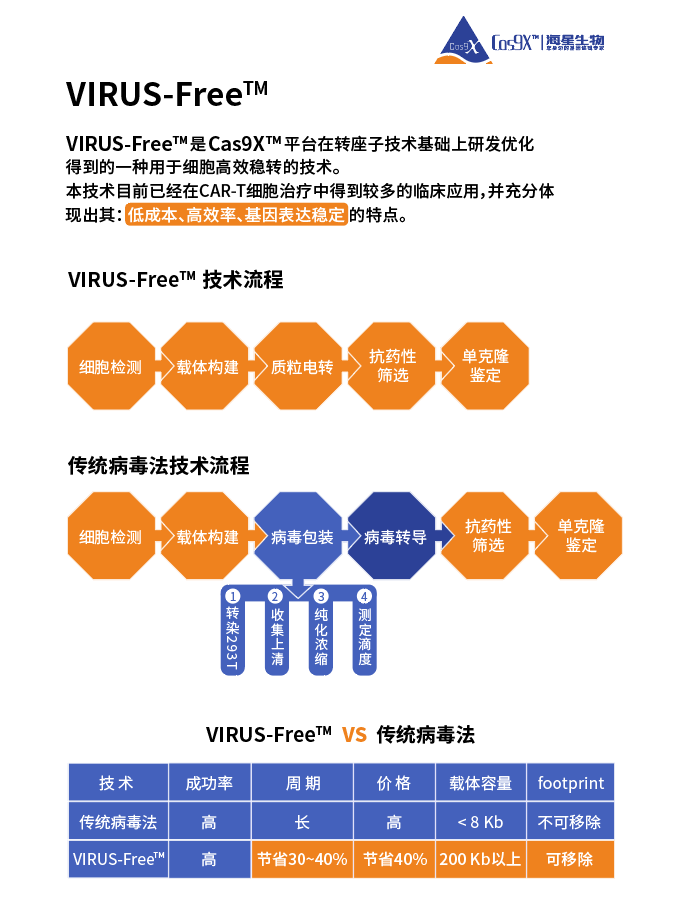
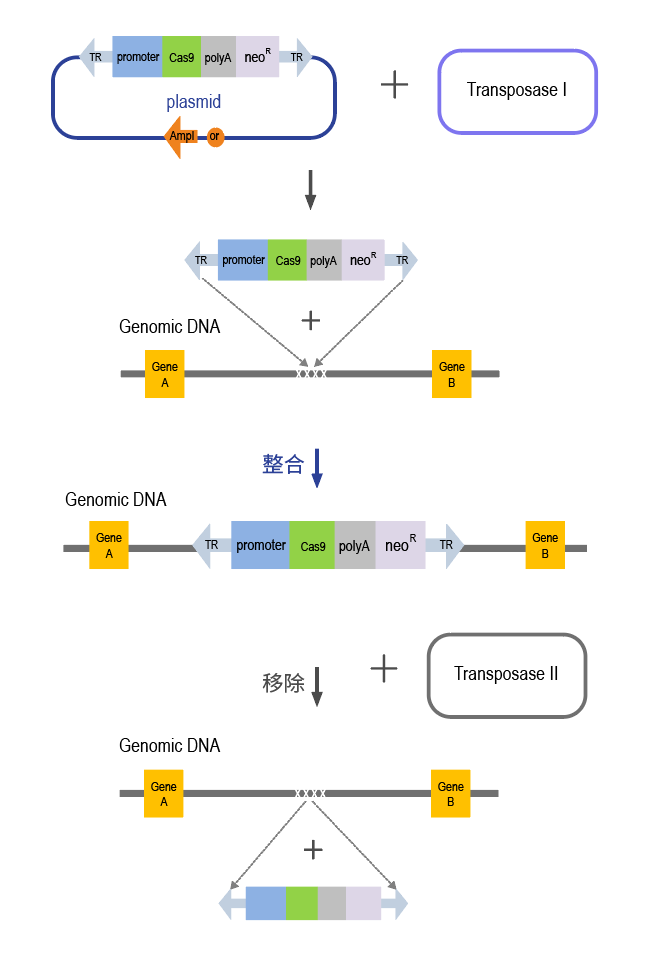
海星生物通过不断探索,开发的VIRUS-Free技术通过构建转座系统质粒,将质粒转染细胞,在转座酶的作用下,高拷贝的Cas9蛋白与sgRNA表达元件被整合到基因组上,比传统的病毒法节省了3-4周,价格节省了约40%。随着基因编辑技术的发展,海星生物将紧随科技发展的步伐,为您的科学研究保驾护航。
参考文献
Knott GJ, Doudna JA. CRISPR-Cas guides the future of genetic engineering. Science. 2018 Aug 31;361(6405):866-869. doi: 10.1126/science.aat5011.
Bak RO, Gomez-Ospina N, Porteus MH. Gene Editing on Center Stage. Trends Genet. 2018 Aug;34(8):600-611. doi: 10.1016/j.tig.2018.05.004.
Fernández A, Josa S, Montoliu L. A history of genome editing in mammals. Mamm Genome. 2017 Aug;28(7-8):237-246. doi: 10.1007/s00335-017-9699-2.